Система валидации. Прочие определения верификации. Что такое валидация и чем она отличается от верификации
— придание законной силы, утверждение, легализация, ратификация
(общегражданское право);
— процесс, позволяющий определить, насколько точно с позиций потенциального пользователя некоторая модель представляет заданные сущности реального мира
(системное программирование);
— процедура, дающая высокую степень уверенности в том, что конкретный процесс, метод или система будет последовательно приводить к результатам, отвечающим заранее установленным критериям приемлемости; в частности, валидация технологических процессов проводится с использованием образцов не менее трех серий реального продукта с целью доказательство и предоставление документального свидетельства, что процесс (в пределах установленных параметров) обладает повторяемостью и приводит к ожидаемым результатам при производстве полупродукта или готового продукта требуемого качества; валидация аналитических методов состоит в определении: точности, воспроизводимости, чувствительности, устойчивости (межлабораторная воспроизводимость), линейности и других метрологических характеристик
(GMP — Надлежащая производственная практика, является обязательным требованием при производстве лекарственных средств).
Применительно к системам менеджмента качества согласно стандартам ISO серии 9000:
Валидация
— подтверждение на основе представления объективных свидетельств того, что требования, предназначенные для конкретного использования или применения, выполнены
(ISO 9000:2005)
Валидация
— подтверждение путем экспертизы и представления объективного доказательства того, что особые требования, предназначенные для конкретного применения, соблюдены.
Примечания:
- При проектировании и разработке утверждение означает проведение экспертизы продукции с целью определения соответствия нуждам потребителя.
- Утверждение обычно осуществляется на конечной продукции в определенных условиях эксплуатации. Оно может быть необходимо на более ранних стадиях.
- Термин «утверждено» используется для обозначения соответствующего статуса.
- Могут осуществляться многократные утверждения, если предполагается различное использование.
(ISO 8402:1994, п.2.18)
По определению PIC/S, это:
«Действия, которые в соответствии с принципами GMP доказывают, что определенная методика, процесс, оборудование, сырье, деятельность или система действительно приводят к ожидаемым результатам».
Валидация
Исследования по валидации должны способствовать надлежащей практике производства; их следует проводить в соответствии с установленными процедурами. Результаты и заключения должны быть оформлены протоколами.
Если вводят новую производственную рецептуру или новый способ изготовления, то должны быть предприняты действия, демонстрирующие их пригодность для серийного производства. Должно быть доказано, что установленный процесс при использовании специфицированных веществ и оборудования позволяет постоянно получать продукцию требуемого качества.
Существенные изменения производственного процесса, включая любое изменение оборудования или материалов, которое может повлиять на качество продукции и/или воспроизводимость процесса, должны пройти валидацию.
Процессы и процедуры следует подвергать периодической критической ревалидации, чтобы гарантировать, что они по-прежнему способны приводить к ожидаемым результатам.
Валидация и ее документирование
Цель валидации простая: доказать, что объект валидации действительно приводит к ожидаемым результатам. Другими словами, валидация должна показать, что производитель полностью управляет процессом производства. Валидация является интегральной частью «обеспечения качества», показывая, что производитель понимает причины изменчивости процесса и, главным образом, понимает какие параметры необходимо контролировать для обеспечения стабильности процесса. Эффективная валидация основана на менеджменте риска и современном уровне науки.
Процедуры процесса валидации должны быть зафиксированы в ряде протоколов и результаты валидации должны быть зафиксированы в записях или отчетах.
Эти документы используются в разных формах при получении регистрационного удостоверения и инспекции в соответствии с правилами GMP и так же, для внутренних производственных целей, чтобы руководство организации могло быть уверено в том, что оно контролирует свои процессы. Документация процесса валидации является базой для необходимой регуляции. Но для того, чтобы избежать
той ошибки, которая часто встречается при внедрении принципов GMP в России, мы сознательно обсуждаем процесс документирования валидации в разделе о документации.
Существует довольно серьезная разница между российским и международным подходами. В российских правилах GMP, валидация «заключается в документированном подтверждении соответствия оборудования, условий производства, качества сырья и готового продукта действующим регламентам и\или требованиям нормативной документации». Это подход – устаревший. Его последствия – довольно вредные. Из разных публикаций может создаться впечатление, что процесс валидации является не более, чем процессом документирования или, что такие слова как «валидация» «верификация», «квалификация» и «испытание», в самом деле, являются аналогами друг друга. Отсутствие понимания «валидации» укрепляет недопонимание GMP, и создает ситуацию, когда персонал сопротивляется внедрению GMP, просто принимая его как «вечно растущую гору документов».
В GMP EC (и, кстати, GMP FDA) валидация является регулярным изучением систем, процессов, инженерных комплексов и, естественно, самого фармацевтического продукта, чтобы обеспечить высокий уровень уверенности в том, что процессы были должным образом разработаны и находятся под контролем.
Эффективная валидация требует использования подхода, основанного на управлении рисками, полного понимания процессов производства и повышения их устойчивости, посредством внедрения новых технологий. Таким образом, валидация является динамическим процессом. Этот факт, очевидно, представляет некоторые сложности для регуляторных органов.
С точки зрении разработчиков и производителей ЛС валидация способна обеспечить следующие преимущества:
- более глубокое понимание процессов и поэтому, уменьшение риска при предотвращении проблем и обеспечение гладкого управления процессом;
- снижение стоимости устранения недостатков;
- уменьшение риска несоответствия требованиям регуляторных органов.
После полной валидации процесса, возможно, что количество контролируемых параметров в конце процесса уменьшится. Разработчики, полностью понимая те параметры, которые влияют на изменчивость и, следовательно, на стабильность процесса, имеют необходимую информацию для управления процессом, например, через снижение изменчивости или повышение его скорости. Хотя «валидация» является интегральной частью «обеспечения качества», здесь видна взаимосвязь между валидацией и системой менеджмента. Для того чтобы эффективно проводить валидацию, руководство компании должно определить свою политику в данном вопросе. Одним из первых элементов, который инспектор FDA или PIC/S на-мерен проверить, является именно политика валидации.
Сложности интерпретации требований ИСО 9001 в отношении «валидации специальных процессов» известны каждому менеджеру по качеству, который хоть раз сталкивался с внедрением этого стандарта. Вот и получается на практике, что вполне стандартное требование, четко и подробно описанное в нормативных документах для фармацевтической отрасли, для других отраслей сопровождается пугающим количеством толкований и разъяснений. Выдержка из ИСО 9001, пункт 7.5.2: «Организации следует осуществлять валидацию любого процесса выпуска продукции или предоставления услуг, подтверждение (верификацию) конечного выхода которого невозможно провести последующим мониторингом или измерениями, и следовательно, недостатки которого (т.е. конечного выхода) выявляются только после начала использования продукта или завершения оказания услуги» . И соответственно в стандарте ИСО 9000:2005 в 3-м примечании к определению термина «процесс» (3.4.1) указано, что «Процесс, в котором подтверждение (верификация) соответствия конечной продукции не может быть проведено своевременно или влечет к значительным экономическим затратам, часто называют специальным» .
Для фармацевтической отрасли под определение специального процесса полностью подпадает «технологический процесс», т.е. процесс изготовления лекарственного препарата. Естественно предполагается, что препарат качественный. Что такое «качество лекарственного препарата»? Прежде всего, это его эффективность , безопасность и соответствие спецификации (стандарту качества). Соответствие спецификации можно подтвердить контролем качества (по сути, верификацией), однако проблема в том, что контроль выборочный. Т.е. результаты контроля распространяются на всю серию на основании тестирования образцов, которые не идут в продажу. И это еще большая задача, доказать что выборка – репрезентативна. Дальше еще хуже. Безопасность и эффективность лекарственного препарата подтверждаются (или не подтверждаются) только в процессе его применения – т.е. тогда, когда что-то изменить, исправить уже невозможно.
Именно поэтому одним из ключевых принципов (G ood M anufacturing P ractice, ) считается технологического процесса. Валидации процессов посвящено отдельное приложение – Приложение 15 , которое было включено в в 1987 году. И что очень важно, без результатов валидации коммерческий выпуск лекарственного препарата невозможен, правильнее сказать жестче – запрещен. поддерживает концепцию GMP в переносе центра тяжести с контроля качества готового продукта на обеспечение качества процесса . Кроме того, процедуры организации и проведения валидации отражают базовые принципы GMP, а именно: продуманное планирование, четкое выполнение и подробное документирование. включает такие важные для GMP элементы, как научный подход на основе оценки рисков по качеству и управление изменениями.
Что такое валидация?
Корень «валид» означает пригодный. В русском языке есть несколько слов с этим корнем, например «инвалид» — непригодный, «валидный» — пригодный. В фармацевтической отрасли, термин «валидация» трактуется следующим образом: «Процесс документированного подтверждения достижения разумной степени уверенности в том, что
— Производственный процесс,
— Аналитические методики,
— Используемое оборудование,
— Производственные системы,
соответствуют действующим принципам GMP и выполняют свое функциональное назначение, т.е. их использование действительно дает ожидаемые результаты ».
По сути, валидация технологического процесса – это конечная цель, для достижения которой нужно последовательно провести валидацию ряда других связанных процессов. В GMP общий термин «валидация» разделяется на два понятия: «валидация процессов» и «квалификация производственных систем». Квалификация производственных систем – это часть валидации процесса, направленная на документальное подтверждение пригодности оборудования, инженерных систем, комплекса помещений, которые используются в производстве лекарственного препарата. Квалификация проводится для того, чтобы быть уверенными в том, что производственная система не влияет на качество продукта, а также для того, что если мы в ходе непосредственно валидации технологического процесса получим негативный результат – это не может быть связано с отказами оборудования/систем, а причины нужно искать в самом технологическом процессе). По своей логике, квалификация производственных систем – это некая предупреждающая мера.

Таким образом, под валидацией процесса в фармацевтической отрасли подразумевается :
— Квалификация чистых помещений
— Квалификация инженерных систем (подготовка чистого воздуха, воды очищенной и воды для инъекций, сжатого воздуха и т.п.)
— Квалификация производственного оборудования
— Квалификация аналитического оборудования (используемого для контроля качества сырья, полупродуктов и готовой продукции)
— Квалификация складских зон (сырье, готовая продукция)
— Валидация компьютеризированных систем, включая квалификацию ИТ-инфраструктуры
— Валидация аналитических методик
— Валидация очистки помещений, оборудования
— Валидация асептических условий
— Валидация этапов технологического процесса
— Валидация упаковки
Организация валидационных работ
Ответственность за проведение валидационных работ как правило возложена на Отдел обеспечения качества. Для координации деятельности структурных подразделений создается Валидационная комиссия и валидационные группы.
Документальное сопровождение
Стандартный пакет валидационной документации:
— Валидационный мастер-план (или Общий план валидации)
— Валидационное досье (отдельно для каждого объекта): Спецификация требований пользователя (URS, U ser R equirement S pecification); Протокол оценки рисков; Программа (сценарий) валидационных работ; Протокол/Отчет валидационных работ; Программа (плановой, внеплановой) ревалидации (повторной валидации)
Квалификация
Для каждого критического объекта инфраструктуры должна быть проведена квалификация, которая, как правило, осуществляется в четыре последовательных этапа:
(DQ) подтверждение пригодности проекта (конструкции, проектного решения) технических средств, инженерных систем и оборудования для их предполагаемого использования. Объем работ на этом этапе:
— Описание системы (функция, параметры оборудования, особые характеристики)
— Техническая документация (нормативные требования, документация по оборудованию)
— Оценка конструкции (конструкционные материалы, оценка риска загрязнений)
— Компоненты/элементы оборудования/системы
— Анализ возможных отказов/дефектов
— Анализ способа изготовления (критические параметры работ при изготовлении оборудования, требования по калибровке)
(IQ)
направлена на документированное подтверждение
того,
что технические средства, инженерные системы и оборудование сконструированы, оснащены и смонтированы в соответствии с рабочей документацией проекта и рекомендациями производителя.
Объем работ на этом этапе:
— Наличие достаточной документации
— Наличие всех элементов в поставке
— Правильность монтажа и подключений
— Соответствие контактирующих материалов
— Соответствие средств измерений
(OQ)
направлена на документированное подтверждение
того, что технические средства, инженерные системы и оборудование функционируют должным образом по всему заявленному диапазону
рабочих характеристик. Объем работ на этом этапе:
— Приемлемость документации (инструкции по эксплуатации, обслуживанию);
— Испытания, включающие условие или ряд условий, охватывающих верхний и нижний пределы рабочих параметров:
— Срабатывание блокировок/сигнализаций.
Как правило, после этого этапа квалификации объект вводится в эксплуатацию.
Квалификация функционирования () проводится для инженерных систем, которые работают непрерывно, а также для оборудования со сложным управлением. Квалификация в эксплуатации – это документированное подтверждение того, что технические средства, инженерные системы и оборудование при совместном (или длительном) использовании могут надежно функционировать с получением воспроизводимых свойств продукта .
При этом, если производственная система оснащена автоматизированной системой мониторинга параметров, или обработки данных, дополнительно должна проводиться валидация компьютеризированной системы .
Валидация аналитических методик
Каждая аналитическая и микробиологическая методика, которая используется для контроля качества сырья, полупродукта или готового продукта должна пройти валидацию. Это означает, что мы обязаны получить доказательства пригодности такой методики для контроля конкретного продукта и соответственно, гарантии получения достоверных результатов. В этом плане, требования GMP полностью совпадают с требованиями ИСО 17025.
Валидация очистки
Процедуры очистки оборудования должны также пройти валидацию до того, как мы приступим к производству препарата на этом оборудовании. Прежде всего, эта валидация направлена на получение гарантий возможности проведения качественной очистки после изготовления такого продукта. По сути, это минимизация риска перекрестного загрязнения при переходе на производство другого продукта на этом же оборудовании. Если на оборудовании останутся остатки предыдущего продукта, это не будет обнаружено – так как отсутствует аналитический контроль именно на наличие таких примесей.
Валидация асептических условий
При производстве стерильных лекарственных средств с использованием асептических технологий до начала самого технологического процесса необходимо подтвердить, что на всем протяжении процесса изготовления препарата (т.е. длительность процесса), в продукт не попадает ни один микроорганизм. Валидация асептических условий проводится по сценарию имитации с помощью питательных сред.
Валидация технологического процесса
И непосредственно, валидация каждого из этапов технологического процесса проводится на 3-х последовательных сериях с учетом «наихудшего случая». И, что очень важно, валидация технологического процесса проводится отдельно для каждого продукта и его заявляемого размера серии. Наихудший случай – это проведение процесса при таких условиях и обстоятельствах (для параметров процесса, режимов работы оборудования), которые имеют максимальные шансы вызвать отклонение процесса или несоответствие продукта по сравнению с идеальными условиями. Логика очень проста – если при таких условиях мы получаем качественный продукт, значит, гарантированно мы будем достигать качества внутри заданных диапазонов.
Повторная валидация/квалификация
Через заданные периоды эксплуатации (использования), каждый объект/процесс должны пройти повторную валидацию. Основная цель повторной валидации (ревалидации) – это получить подтверждения того, что объект/процесс продолжает находиться в валидном состоянии. Это полностью отражает логику GMP: «Для подтверждения качества продукта недостаточно провести валидацию в начале его жизненного цикла, необходимо обеспечить мониторинг и постоянное улучшение» (см. схему ниже).

Рассматривается плановая и внеплановая ревалидация. Плановая – проводится по графику в соответствии с заранее установленной периодичностью (как правило, через 12-24 мес.). Внеплановая ревалидация – после длительных простоев, при появлении тренда отклонений или при внесении изменений.
Перечень приведен в той последовательности, в которой должны проводиться валидационные работы
13-й международный проект «Созвездие качества’2012»
Александр В. Александров, Группа компаний ВИАЛЕК
Тезисы доклада
Добрый день сегодня я расскажу вам «Что такое валидация аккаунта в контакте?». Валидация аккаунта – это подтверждение вашей страницы с помощью телефона. Объясняю, чтобы восстановить пароль или изменить имя, социальная сеть Вконтакте будет присылать бесплатное смс с кодом на телефон указанный вами. После ввода этого кода на сайте ваш пароль или имя будут изменены.
Данный способ намного надежней , чем обычное восстановление пароля через почту. Так как хакерам намного легче взломать ваш почтовый ящик, чем получить доступ к вашему телефону.
Зачем нужна валидация аккаунта?
Как вы могли догадаться, валидация аккаунта требуется для уменьшения заражённых страничек с помощью, которых:
- Рассылают спам.
- Похищают личную информацию.
- Обворовывают и обманывают пользователей.
Если раньше валидация вконтакте была необязательной, то теперь она является обязательной при регистрации. Если у вас нет номера телефона, то зарегистрироваться в контакте у вас не получиться. Я советую всем подтверждать свои аккаунты с помощью валидации, так как при взломе и похищении страницы, вы сможете её быстро вернуть . О том, как вернуть страницу Вконтакте я писал .
Вирус или валидация?
А теперь самое интересное, существует вирус, который очень часто подхватывают пользователи социальной сети Вконтакте. Его можно подхватить разными способами, например:
- Вы перешли по странной .
- Скачали непроверенную программу.
- Попали на фишинговый сайт и т.д.
Вирус этот очень подлый, так как он притворяется валидацией аккаунта и просит отправить бесплатное смс.
Валидация аккаунта как убрать?
Если вы у вас появляется окошко валидации, то это 100% вирус. Так как Вконтакте просит валидацию аккаунта, только при регистрации. Пожалуйста, не нужно писать, что у вас не заходит вконтакте, я все равно посоветую вам проверить компьютер на вирусы. Если же у вас более интересный вопрос, спрашивайте, я отвечу. Вернёмся к вопросу как убрать валидацию аккаунта, по этой теме я уже написал три статьи. С помощью первой вы научитесь уничтожать вирус вручную, в остальных я рассказывал, как скачать, настроить и запустить антивирус, который быстро справиться с вирусами. Вот эти три статьи:
Советую использовать антивирус, это сэкономит ваше время и силы. Если у вас вопросы типа, что значит валидация аккаунта?, то прочитайте ещё раз статью. Ну а если по делу, задавайте их в комментариях!
Если вам помогла или понравилась данная статья, не забудьте поставить свой лайк , это поможет другим пользователям найти её быстрей. А я смогу узнать, что интересует вас больше всего, чтобы подготовить и написать еще больше интересных и полезных статей! С уважением, Вячеслав.
Придание законной силы, утверждение, легализация, ратификация
(общегражданское право
);
Процесс, позволяющий определить, насколько точно с позиций потенциального пользователя некоторая модель представляет заданные сущности реального мира
(системное программирование
);
Процедура, дающая высокую степень уверенности в том, что конкретный процесс, метод или система будет последовательно приводить к результатам, отвечающим заранее установленным критериям приемлемости; в частности, валидация технологических процессов проводится с использованием образцов не менее трех серий реального продукта с целью доказательство и предоставление документального свидетельства, что процесс (в пределах установленных параметров) обладает повторяемостью и приводит к ожидаемым результатам при производстве полупродукта или готового продукта требуемого качества; валидация аналитических методов состоит в определении: точности, воспроизводимости, чувствительности, устойчивости (межлабораторная воспроизводимость), линейности и других метрологических характеристик
(GMP - Надлежащая производственная практика, является обязательным требованием при производстве лекарственных средств
).
Применительно к системам менеджмента качества согласно стандартам ISO серии 9000:
Валидация - подтверждение на основе представления объективных свидетельств того, что требования, предназначенные для конкретного использования или применения, выполнены (ISO 9000:2005 )
Валидация
- подтвержение путем экспертизы и представления объективного доказательства того, что особые требования, предназначенные для конкретного применения, соблюдены.
Примечания:
1. При проектировании и разработке утверждение означает проведение экспертизы продукции с целью определения соответствия нуждам потребителя.
2. Утверждение обычно осуществляется на конечной продукции в определенных условиях эксплуатации. Оно может быть необходимо на более ранних стадиях.
3. Термин «утверждено» используется для обозначения соответствующего статуса.
4. Могут осуществляться многократные утверждения, если предполагается различное использование.
(ISO 8402:1994, п.2.18
)
Проведем анализ требований стандарта ISO 9001:
ISO 9001, п. 7.3.6: Валидация проекта и разработки должна осуществляться в соответствии с запланированными мероприятиями, чтобы удостовериться, что полученная в результате продукция соответствует требованиям к установленному или предполагаемому использованию.
ISO 9001, п. 7.5.2: Валидация процессов производства и обслуживания. Организация должна подтверждать все процессы производства и обслуживания, результаты которых нельзя проверить посредством последовательного мониторинга или измерения. К ним относятся все процессы, недостатки которых становятся очевидными только после начала использования продукции или после предоставления услуги. Валидация должна продемонстрировать способность этих процессов достигать запланированных результатов.
ISO 9000, примечание 3 п. 3.4.1: Процесс, в котором подтверждение соответствия конечной продукции затруднено или экономически нецелесообразно, часто относят к "специальному процессу
".
Общепринятые требования к специальным производственным процессам
, обеспечивающие их валидацию:
1) аттестация производственного процесса (технология, методика, рабочие инструкции...)
2) аттестация производственного оборудования (калибровка сварочных машин или роботов, краскопультов и систем подачи краски...)
3) аттестация материалов (электроды, газ, флюсы, краска, растворители, грунты...)
4) аттестация персонала (квалификационные требования к сварщикам или операторам сварочных роботов, наладчикам, сервисным компаниям...)
с соответствующим документальным подтверждением. (А.Орешин
)
Спец. процесс (СП) должен быть в управляемых условиях.
Управляемые условия включают:
- наличие информации, описывающей характеристики продукции и СП;
- наличие нормативной, конструкторской и технологической документации;
- использование пригодного оборудования;
- наличие и использование средств контроля и измерений;
- проведение контроля, измерений и испытаний;
- осуществление деятельности по выполнению СП;
- наличие квалифицированного и аттестованного персонала осуществляющего СП;
- повторную валидацию;
- наличие записей, содержащих достигнутые результаты или свидетельства осуществленной деятельности при выполнении СП. (В.Золотухин
)
Валидация, верификация, специальный процесс
Чем отличается валидация от верификации?
Стандарт ИСО 9000 определяет эти термины следующим образом:
"Верификация
- подтверждение на основе представления объективных свидетельств того, что установленные требования были выполнены".
"Валидация
- подтверждение на основе представления объективных свидетельств того, что требования, предназначенные для конкретного использования или применения, выполнены".
Казалось бы, определения чуть ли не совпадают и уж если не полностью, то в значительной части. И, тем не менее, верификация и валидация - принципиально разные действия.
Разберемся.
Уже перевод с английского этих терминов дает определенную пищу для понимания разницы: verification - проверка, validation - придание законной силы.
Чтобы было проще понять, сразу приведу пример типичной верификации: тестирование программы или проведение испытания оборудования. Имея определенные требования на руках, мы проводим испытание продукта и фиксируем, соблюдены ли требования. Результат верификации - это ответ на вопрос "Соответствует ли продукт требованиям?".
Но далеко не всегда продукт, соответствующий установленным требованиям, можно применять в конкретной ситуации. Например, лекарство прошло все положенные испытания и поступило в продажу. Значит ли это что оно может быть применено каким-то конкретным больным? Нет, т.к. каждый пациент имеет свои особенности и конкретно для этого лекарство может быть губительным, т.е. кто-то (врач) должен подтвердить: да, этому больному можно принимать это лекарство. То есть врач должен выполнить валидацию: придать законную силу конкретному применению.
Или еще пример. Предприятие выпускает трубы, предназначенные для закладки в землю, в соответствии с некоторыми ТУ (Техническими условиями). Продукция этим ТУ соответствует, но поступил заказ, предполагающий укладку труб по дну моря. Могут ли трубы, соответствующие имеющимся ТУ, быть применены в данном случае? Именно валидация и дает ответ на этот вопрос.
Нетрудно видеть, что еще одно отличие состоит в том, что верификация производится всегда, а вот необходимость в валидации может и отсутствовать. Она появляется только тогда, когда возникают требования, связанные с конкретным применением продукции. Если фармацевтический завод выпускает лекарства, то он будет проверять лишь их соответствие требованиям, а проблемами применения конкретных лекарств конкретными пациентами заниматься не будет. Или тот же АвтоВАЗ.
Таким образом, можно констатировать следующее:
верификация - проводится практически всегда, выполняется методом проверки (сличения) характеристик продукции с заданными требованиями, результатом является вывод о соответствии (или несоответствии) продукции,
валидация - проводится при необходимости, выполняется методом анализа заданных условий применения и оценки соответствия характеристик продукции этим требованиям, результатом является вывод о возможности применения продукции для конкретных условий.
Стандарт ИСО 9001 в двух местах обращается к этим терминам. Проверим, соответствует ли данное мной толкование содержанию разделов 7.3.5, 7.3.6 и 7.5.2.
"7.3.5. Верификация проекта и разработки. Верификация должна осуществляться в соответствии с запланированными мероприятиями (п. 7.3.1), чтобы удостовериться, что выходные данные проектирования и разработки соответствуют входным требованиям:".
"7.3.6. Валидация проекта и разработки. Валидация проекта и разработки должна осуществляться в соответствии с запланированными мероприятиями (п. 7.3.1), чтобы удостовериться, что полученная в результате продукция соответствует требованиям к установленному или предполагаемому использованию, если оно известно. Где это практически целесообразно, валидация должна быть завершена до поставки или применения продукции".
Нетрудно видеть, что моя трактовка находится в полном согласии с текстом этих разделов. При этом хотелось бы обратить внимание на то, что в п. 7.3.5 говорится о соответствии выходных данных, а в п. 7.3.6 - продукции. Это существенно! Это означает, что валидация проводится не для выходных данных, а для разработанной под конкретные условия продукции. Скажем, в деятельности института по разработке типовых проектов жилых зданий валидация не требуется - только верификация. А вот для деятельности по разработке проекта строительства жилого здания по тому же типовому проекту, но в конкретном месте, валидация уже необходима.
"7.5.2. Валидация процессов производства и обслуживания. Организация должна подтверждать все процессы производства и обслуживания, результаты которых нельзя проверить посредством последовательного мониторинга или измерения. К ним относятся все процессы, недостатки которых становятся очевидными только после начала использования продукции или после предоставления услуги. Валидация должна продемонстрировать способность этих процессов достигать запланированных результатов".
Здесь также нет расхождений. Но при этом следует заметить, что в случаях, подпадающих под п. 7.5.2 характеристики продукции не могут быть измерены напрямую и их оценка будет проводиться косвенно (подробнее см. лекцию о специальных процессах).
Вопрос
: к чему отнести деятельность ОТК?
Ответ
: это верификация.
Вопрос
: к чему отнести деятельность аудиторов?
Ответ
: к верификации.
Вопрос
: какую функцию выполняет подписывающий акт о сдаче в эксплуатацию объекта (услуги и т.п.)?
Ответ
: он осуществляет валидацию.
Определение специального процесса
Критерии отнесения процесса к "специальным"
Безусловно, правы те, кто говорит, что стандарт впрямую не определяет термина "специальный процесс". Это словосочетание встречается в Примечании 3 п. 3.4.1 ИСО 9000 "Процесс, в котором подтверждение соответствия конечной продукции затруднено или экономически нецелесообразно, часто относят к "специальному процессу
".
То есть здесь главным признаком "специальности" выступает затрудненность (проблематичность) подтверждения соответствия. Конечно, вряд ли такой критерий можно считать однозначным, так как неясна мера затрудненности, при превышении которой процесс уже можно считать "специальным".
С другой стороны, п. 7.5.2 стандарта ИСО 9001 устанавливает требование: "Организация должна подтверждать все процессы производства и обслуживания, результаты которых нельзя проверить посредством последовательного мониторинга или измерения
".
Попробуем ответить на несколько вопросов, первый из которых: а зачем п. 7.5.2 вообще включен в стандарт ИСО 9001? Или иными словами: каково практическое значение подтверждения (валидации) процессов для менеджмента качества?
Цель системы менеджмента качества (по ИСО 9001) - обеспечить стабильное качество продукции, понимаемое как соответствие требованиям потребителя. С этой точки зрения всякий процесс производства мы можем назвать результативным (качественным), если его результат соответствует заданным требованиям.
Но вот вопрос: а как быть, если результат не может быть непосредственно сравнен с требованиями (измерен)? Как определять результативность такого процесса? Вот тут-то на сцену и выходит п. 7.5.2, который говорит, что такие процессы должны "подтверждаться" (валидироваться), чтобы "продемонстрировать способность этих процессов достигать запланированных результатов". Т.е. не можешь проверить результат, тогда подтверди "правильность" процесса, исходя из предположения, что "правильный" процесс дает "правильный" результат.
Между положениями Примечания 3 п. 3.4.1 ИСО 9000 и п. 7.5.2 стандарта ИСО 9001 есть очевидная общность: и то, и другое относится к подтверждению соответствия продукции. Но есть и столь же очевидная разница: если ИСО 9000 говорит о "затрудненности" (никак не определяя ее меру), то ИСО 9001 более категоричен: "нельзя проверить", т.е. речь идет о "невозможности".
Так можно ли процессы, в отношении которых устанавливаются требования в п. 7.5.2 считать теми самыми "специальными" процессами? Я полагаю, да, т.к. "невозможность" - это крайняя степень "затрудненности".
Практическая значимость принятия решения об отнесении процесса к "обычным" или "специальным"
Отнесение (или не отнесение) процесса к "специальным" имеет практическое значение и выполняется в рамках планирования процесса, предусмотренного разделом 7.1 стандарта ИСО 9001.
Дело в том, что, как я постараюсь показать далее, "обычный" и "специальный" процесс строятся различным образом и это различие в построении объясняется разной методикой определения результативности процесса. Не вдаваясь в тонкости, можно сказать, что результативность "обычного" процесса оценивается соответствием результата заданным требованиям, а результативность "специального" процесса - соответствием действий, выполненных в рамках процесса, установленной технологии. Говоря иными словами, "обычный" процесс мы назовем результативным, когда его выход соответствует заданным требованиям, а "специальный" - когда технология получения выхода соответствует установленной. Поэтому выстраивая "обычный" процесс, мы должны предусмотреть в нем операции мониторинга соответствия требованиям результатов на промежуточных и конечной стадиях производства, основанные на измерениях этих результатов. А при построении "специального" процесса приоритеты будут другими: мы включим в него операции мониторинга соответствия технологии производства, основанные на записях о соблюдении технологии.
Можно ли процесс предоставления услуги считать специальным?
Пункт 7.5.2 содержит указание: "К ним
["специальным"] процессам относятся все процессы, недостатки которых становятся очевидными только после начала использования продукции или после предоставления услуги
".
Как показывает практика, это положение не имеет однозначного трактования в среде специалистов по менеджменту качества и требует отдельного анализа, особенно в той части, что касается услуг.
Во-первых, хотел бы заострить внимание на том, что положение говорит о недостатках процесса, а не продукции.
Во-вторых, хотел бы двумя следующими блок-схемами показать принципиальное отличие процесса производства материальной продукции от процесса производства услуги.

Здесь самое время определить, что такое услуга
. Под услугой буду понимать деятельность производителя, удовлетворение требований потребителя при которой достигается выполнением действий, а не передачей потребителю материальной продукции. Это определение вполне согласуется с широко распространенным положением, что при оказании услуги ее производство и потребление совпадают во времени.
Размышления о природе процесса оказания услуг приводит нас к пониманию того, что
- результатом процесса оказания услуги является потребленная услуга, т.е. услуга, процесс производства и потребления которой завершился,
- потребитель является участником процесса оказания услуги (находится "внутри" процесса),
- попытка вынести потребление услуги за границы процесса оказания услуг приводит к "исчезновению" выхода и, соответственно, самого процесса.
Последнее положение указывает на то, что в точке А (второй рисунок) услуги, как результата всей совокупности действий, еще нет - ведь потребление происходит в процессе производства.
Следующий вопрос, на который необходимо ответить: применимо ли к процессу оказания услуги понятие "мониторинг или измерение [результата]".
Очевидно, что да. Те же телекоммуникационные услуги дают нам такой пример: клиенту организован канал, по которому идет сигнал клиента и все оговоренные параметры отслеживаются. А после завершения оказания услуги мы на основании данных мониторинга и измерений сможет сказать, был ли процесс результативным или нет. Вот ключевой момент: для установления результативности процесса мы не будем анализировать записи о выполнении (или не выполнении) тех или иных действий, о соответствии этих действий запланированным, а мы будем анализировать записи о параметрах услуги, т.е. данные о результате. Говоря иными словами, если клиент недоволен, то мы в свою защиту не станем демонстрировать ему, что все предусмотренные технологией операции были выполнены в точном соответствии с инструкциями, а покажем результаты мониторинга и измерений параметров услуги. И это самым очевидным образом говорит нам о том, что рассматриваемый процесс оказания услуги никак не может быть отнесен к специальным.
Примеры демонстрации применения на практике обсуждаемых критериев
Дабы подкрепить рассуждения примерами, начнем с услуг.
Ситуация первая
. Имеется экспедиторская компания, оказывающая услуги по доставке. Она решает в состав доставляемых грузов включить мебель. Необходимо спланировать процесс, что вызывает необходимость понять, будет ли процесс "обычным" или "специальным". Основные параметры услуги: точность доставки (время и место), сохранность груза. Могут ли эти параметры быть оценены (измерены)? Конечно, никаких к тому препятствий. Можем мы подтвердить результативность процесса, основываясь на данных оценки (измерения)? Никаких сомнений. Вывод - процесс "обычный".
Ситуация вторая
. Та же экспедиционная контора решила взять на себя заботу по доставке почты Робинзону. При этом корабль близко к острову подойти не может, почта выстреливается катапультой и место ее приземления не всегда видно. Параметры услуги те же. Нетрудно видеть, что в этом случае не все параметры могут быть измерены или оценены: например, место доставки (то ли в болото упала посылка, то ли на дереве повисла) или сохранность. И в отсутствие данных о результате, о результативности процесса будем судить по выполнению технологии: тетиву натянули с нужным усилием, угол возвышения выставили заданный, азимут выставили точно, поправку на ветер внесли и т.д. - т.е. сделали все, чтобы получить заданный результат. Вывод - процесс "специальный".
Ситуация третья
. Мы производим продукцию - ну, скажем, бытовые велосипеды - и у нас есть возможность на каждом этапе производства измерять параметры деталей или узлов и отслеживать их соответствие требованиям. Перед тем, как отдать велосипед потребителю, мы проведем финальную проверку и скажем: вот изделие, оно полностью соответствует установленным требованиям. Нетрудно видеть, что такой процесс мы отнесем к обычным.
Ситуация четвертая
. По заказу NASA мы делаем велосипед для езды на Марсе. При этом одно из требований гласит: соединения должны иметь специальную смазку, после нанесения которой должна быть выполнена сборка и изделие помещено в герметичный контейнер с особой газовой средой. Очевидно, что такое требование лишает нас возможности произвести окончательную проверку велосипеда и при планировании процесса мы должны признать его "специальным". В этом случае, выполняя положения п.п. 7.1 в) и г) мы предусмотрим сбор записей о соблюдении технологии и подтверждение в конце производственного цикла на основе этих записей, что все было сделано "как надо". Это подтверждение, в свою очередь, послужит свидетельством (хоть и косвенным), что результат процесса соответствует требованиям.
Часто можно встретить утверждения вроде "сварка - это специальный процесс" или "окраска - это специальный процесс". На мой взгляд, такие утверждения не совсем корректны.
Будем считать, что результатом сварки является сварочный шов. У нас обычный заказ: трубы для наземного газопровода и все требования обычны. Что мешает проверить все параметры шва при нынешней диагностической технике? Наверно, ничего. Т.е. мы вполне можем установить (подтвердить) соответствие результата требованиям "последовательным мониторингом или измерениями". Но вот пришел иной заказ: нам надо сделать шов, который должен немедленно разрываться при определенной нагрузке. Ну, и как мы подтвердим соответствие этому требованию? Процесс из "обычного" тут же превратился в "специальный".
А отсюда вывод: процесс может быть как "обычным", так и "специальным" - в зависимости от требований к результату. Точно так же, как "всегда специальный" процесс может стать "обычным" при появлении новых технологий и приборов диагностики.
И это находит свое подтверждение в том, что раздел. 7.1, говоря о планировании процессов, подчеркивает: "…для конкретной продукции
" (см. п.п. б и в).
Итак, резюме:
- "обычный" и "специальный" процессы разнятся методами подтверждения соответствия результата, а потому, чтобы правильно построить процесс по производства конкретной продукции, необходимо при планировании процесса провести соответствующую классификацию,
- в основу которой должен быть положен признак "невозможность подтвердить соответствие продукции методами измерения и мониторинга ее параметров" (т.е. невозможность подтвердить результативность процесса методами измерения и мониторинга результата),
- применение которого отчетливо показывает несостоятельность распространенного убеждения: все процессы оказания услуг - "специальные". (А. Горбунов)
Фармацевтикой в ЕС в соответствии с принципами GMP принято определение, согласно которому
валидация
- это формулирование доказательства того, что реализация или использование всех процессов, процедур, оборудования, сырья, продуктов, деятельностей или систем действительно позволяет достигать ожидаемых результатов.
Процесс валидации состоит из последовательности различных квалификаций.
Квалификация
- это операция, предназначенная для того, чтобы доказать, что оборудование правильно работает и действительно дает ожидаемые результаты. Иногда концепт валидации расширяют, чтобы включить в него концепт квалификации.
Валидация состоит из таких процессов:
- квалификация проектной документации (Design Qualification - DQ) - проверка описания и разработки системы;
- квалификация инсталляции (монтажа) (Installation Qualification - IQ) - проверка способности инфраструктуры системы поддерживать работу системы;
- квалификация функционирования (Operational Qualification, OQ) - проверка способности функционировать согласно требованиям;
- квалификация эксплуатации (Performance Qualification - PQ) - проверка способности компании использовать систему.
Здравсвуйте друзья! Поговорим сегодня о такой проблеме, как валидация аккаунта в социальной сети ВКонтакте. Как убрать валидацию и от чего она появляется. Что бы было понятно, давайте сначала разберемся, что такое валидация аккаунта и какая она бывает. Сегодня мы говорим исключительно о социальной сети ВКонтакте, хотя такая проблема очень часто встречается и в Одноклассниках.
Валидация аккаунта – это привязка Вашей страницы к Вашему номеру мобильного телефона. Это нужно для того, что бы можно было легко восстановить доступ к Вашей странице в социальной сети ВКонтакте. Вам просто придет СМС сообщение с кодом, который Вы введете на сайте и получите доступ к своей страничке. В случае, если Вас например взломали, или Вы забыли свой пароль.
ВКонтакте сейчас уже невозможно зарегистрироваться без указания номера Вашего мобильного телефона. А Все ранее созданные странички получили предложение указать номер мобильного телефона, тем самым привязали свою страницу к номеру.
Выше я описал, если так можно сказать, официальный способ валидации аккаунта в социальной сети ВКонтакте.
Вы должны помнить, что ВКонтакте никогда не попросит Вас отправить СМС на короткий (да и на длинный) номер! Валидация – бесплатная. Вы просто вводите свой номер телефона и Вам приходит код, который Вы указывает на сайте для проверки, что тот кто пытается войти на страницу – владелец номера, к которому привязана эта страница.
Но статья не о привязке вашей страницы к номеру, а о вирусах, которые маскируются под “Валидацию аккаунта” и просят Вас отправить СМС на короткий номер, ввести свой логин, пароль, или другие данные. Вот сейчас мы постараемся решить эту проблему и убрать валидацию аккаунта, под которой прячется вирус.
Вы заходите ВКонтакт и видите вот такое окно:
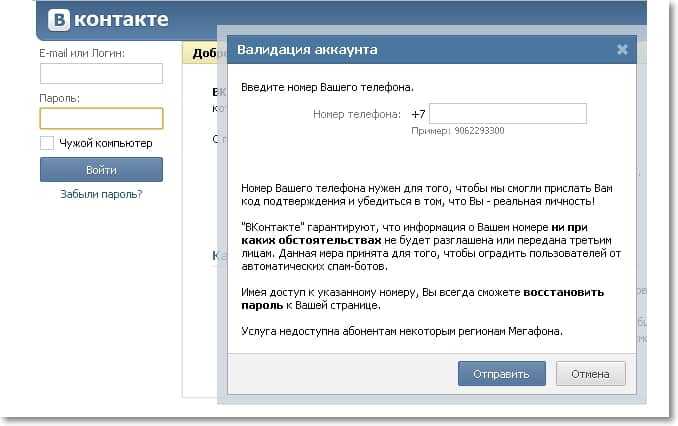
Текст в этом окне может быть другой! Там может быть написано, что Вашу страницу заблокировали и Вам нужно отправить СМС на такой-то номер. Может быть все что угодно. Главное, не отправляйте никаких СМС, скорее всего это вирус!
Проверьте адрес, который прописан в адресной строке браузера. Там должен быть например http://vk.com . Очень часто вирус перенаправляет на другой, похожий адрес, а сам сайт очень похожий на сайт ВКонтакте.
Но так же не стоит забывать, что это может быть и нормальная проверка Вашего номера, которая Вам ничем не угрожает. Сейчас проверим.
Валидация аккаунта ВКонтакте – вирус, или нет?
Для того, что бы проверить, вирус ли это, достаточно попытаться зайти Вконтакт с другого компьютера, или мобильного устройства. Если все нормально и никаких окон с просьбой что-то ввести, или что-то отправить нет, то значит у Вас на компьютере развлекается вирус, который мы попытаемся уничтожить, читайте статью дальше.
Если у Вас нет возможности проверить на другом компьютере, то попробуйте зайти ВКонтакт через анонимайзер, к примеру можно взять . Переходим по ссылке и внизу страницы нажимаем на vk.com.
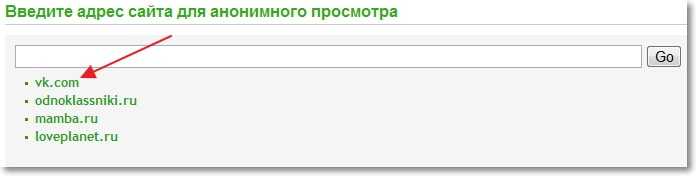
На странице которая откроется, попробуйте войти на свою страницу. Если никаких окон с “Валидация аккаунта” не появится, то значит у Вас на компьютере точно вирус.
Не отправляйте СМС! В лучшем случае, у Вас будет один раз списана определенная сума со счета (примерно 300 рублей, зависит от жадности мошенников). В худшем случае, у Вас после каждого пополнения мобильного телефона будут пропадать деньги с счета.
Как удалить вирус валидация аккаунта ВКонтакте?
Вот мы и подошли к самой интересной части этой статьи. Сейчас я расскажу Вам о некоторых способах, которым можно удалить этот вирус.
Вирусы, которые маскируются под валидацию аккаунта, самые разные и каждый пытается спрятаться как можно глубже в системе, что бы его не нашли. Если говорить о том, где можно поймать такой вирус, то здесь вариантов очень много. Возможно Вы перешли по какой-то ссылке в той же социальной сети ВКонтакте и после этого уже зайти Вконтакте не получается. Возможно Вы скачали какой-то файл и установили его. Вариантов очень много, поймать вирус, это не проблема – проблема от него избавится (правда жизни:)) .
Обычно все вирусы, которые перенаправляют на другие сайты, которые запрещают доступ к определенным сайтам и которые показывают такие окна как “Валидация аккаунта” – изменяют файл hosts. Они могут прописывать туда свои строчки, которые будут Вас перенаправлять на другие сайты, могут создать скрытую копию файла hosts и т. д.
Так же с помощью AVZ можно попытаться вылечить файл hosts. Делается это так:
Запустите утилиту, нажмите на “Файл” и выберите “Восстановление системы” .
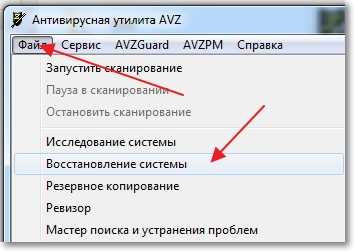
Откроется окно, в котором нужно отметить пункт “Очистка файла hosts” и выбрать “Выполнить отмеченные операции” .

Появится предупреждение, нажмите “Да” .
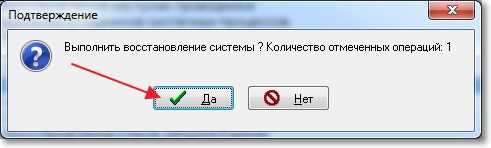
После этих действий перезагрузите компьютер и попробуйте зайти ВКонтакт. Если проблема осталась, то читаем дальше.
Очищаем, удаляем, или заменяем файл hosts
Откройте файл hosts и посмотрите, есть ли в нем ненужен строчки (как должен выглядит файл hosts смотрите ). Этот файл находится в: C:\Windows\System32\Drivers\Etc\ (если у Вас 64-разрядная система, то путь будет таким: C:\Windows\SysWOW64\Drivers\Etc\) .
Вы можете попробовать удалить ненужные строчки открыв его через Блокнот и сохранить файл.
Многие так же просто полностью удаляют папку Etc . Это как правило не страшно для работы системы и помогает решить возникшую проблему. Но эти действия Вы делаете на свой страх и риск!
Бывают случаи, когда вирус создает скрытую копию файла hosts в этой же папке Etc . Вы вносите изменения в файл hosts, но результата нет и это не странно. Решить эту проблему помогает замена самого файла оригиналом.
Нажмите на что бы скачать файл hosts.

Ну с файлом hosts вроде бы разобрались.
Не забудьте еще проверить автозагрузку – Удалите оттуда все странные программы, особенно те, которые имеют расширение.cmd и.bat.
Проверяем DNS-сервер. Возможно вирус заменил его
Подобные вирусы могут изменять DNS сервера. Давайте проверим:
Зайдите в “Пуск” - “Панель управления” - “Центр управления сетями и общим доступом” - “Изменение параметров адаптера” .
Нажмите правой кнопкой мыши на то соединение, через которое Вы подключаетесь к интернету и выберите “Свойства” .
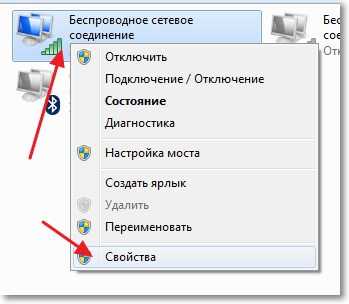
Выделите “Протокол Интернета версии 4 (TCP/IPv4)” и нажмите кнопку “Свойства” .
И посмотрите какой DNS там прописан. Если там какой-то незнакомый Вам адрес, то замените на свой, или установите получать автоматически.

Нужно еще выполнить две команды:
Откройте “Пуск” , “Все программы” , “Стандартные” и запустите Командную строку .
По очереди введите две команды:
route -f
ipconfig /flushdns
После каждой команды подтвердите ее нажатием на Enter .
После этих действий перезагрузите компьютер и попробуйте снова зайти ВКонтакт.
Заключение
Ну вроде бы все основные способы рассмотрел, которыми можно поймать этот вирус. Если у Вас не получилось решить проблему описанными Выше способами, то значит у Вас более серьезный случай. Помню у меня была проблема с Валидацией аккаунта в Одноклассниках (описывал в статье ), решил только переустановкой Windows. Правда тогда много времени разбираться не было. Это я к тому, что переустановка операционной системы помогает:).
Ещё на сайте:
Валидация аккаунта ВКонтакте. Что делать, как решить, это вирус? обновлено: Февраль 7, 2018 автором: admin

